Recordando a escala de pH

RECORDANDO…
Como não podemos andar a provar e mexer em todas as substâncias que encontramos existem testes simples que podem ser efectuados para determinar o carácter químico (ácido, básico ou neutro) das substâncias. Uma das formas de distinguir soluções ácidas de soluções básicas é-lhes adicionando algumas gotas de certas substâncias que mudam de cor, dependendo do carácter químico do meio em que são inseridas. Estas substâncias designam-se por indicadores ácido-base. Neste caso, saber apenas o carácter químico não é suficiente. A
SABER…
Os indicadores de ácido-base apenas permitem separar as substâncias em três grupos – ácidos, substâncias neutras e bases. Ou seja, não nos permitem saber, entre duas substâncias ácidas qual a mais ácida. Para tal é necessário quantificar, isto é, atribuir valores numéricos à acidez e basicidade das soluções de modo a permitir fazer comparações. Para o efeito, foi construída uma escala de referência designada por escala de pH.
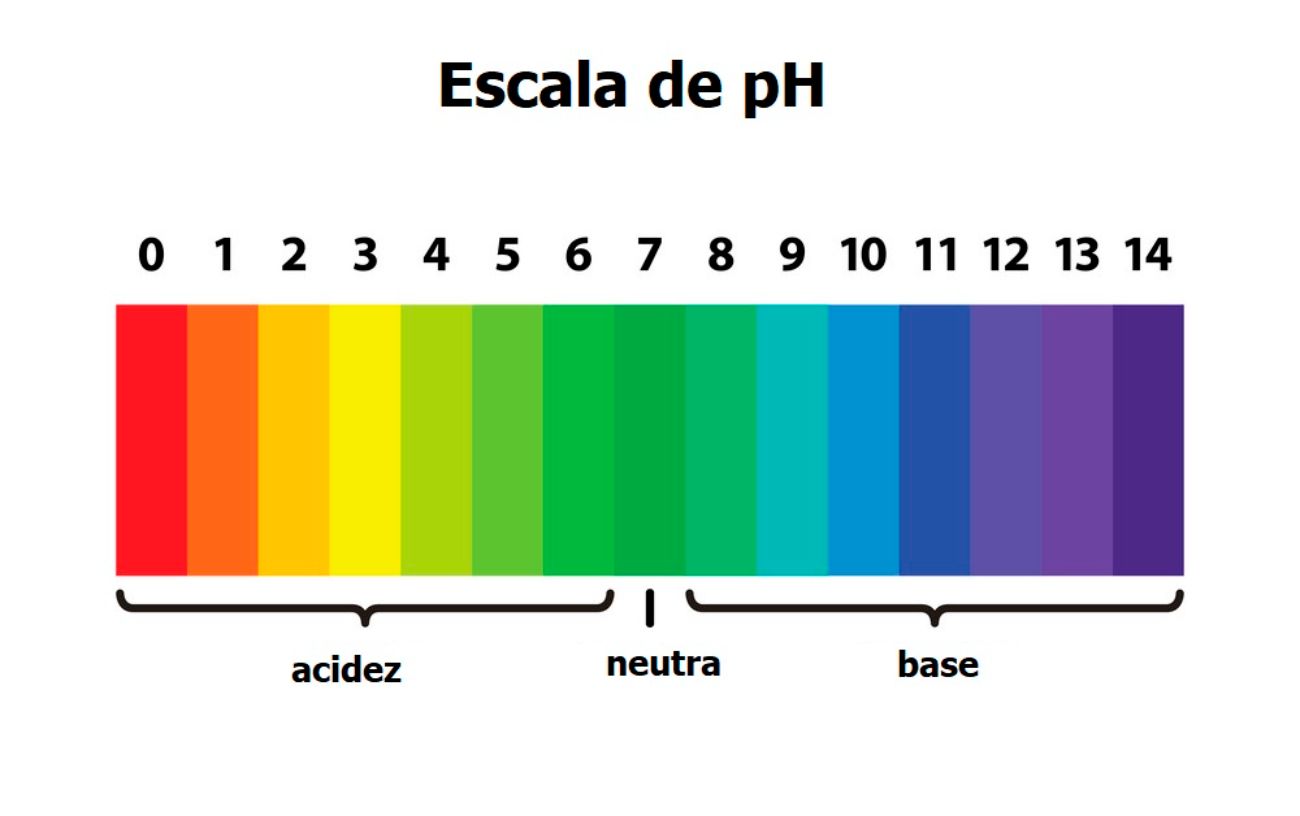
A escala de pH inicia-se no zero e termina no 14. As substâncias neutras têm pH de 7. As substâncias ácidas têm pH abaixo de 7 e as substâncias básica (ou alcalinas) têm pH acima de 7. Quanto mais afastado do 7 mais forte será o carácter químico da substância. De referir que a escala de pH depende da temperatura.
Comentários
Enviar um comentário